Bảng tuần hoàn các nguyên tố hóa học là bảng sắp xếp các nguyên tố dựa trên tính chất hóa học. Dù có một số phiên bản trước đó, phát minh này thường được ghi nhận là của Dmitri Mendeleev, nhà hóa học người Nga, vào năm 1869. Ông tạo ra bảng nhằm thể hiện các xu hướng lặp lại (chu kỳ) trong tính chất nguyên tố. Trải qua thời gian, bảng được mở rộng và hoàn thiện, khi các nguyên tố mới được phát hiện và các mô hình lý thuyết được phát triển để giải thích hành vi hóa học.
Hiện nay, bảng tuần hoàn được sử dụng rộng rãi trong hóa học, và còn ứng dụng trong vật lý, sinh học, kỹ thuật và công nghiệp. Tính đến năm 2006, bảng gồm 117 nguyên tố đã được xác nhận, trong đó 92 nguyên tố có trong tự nhiên, còn lại là nhân tạo.
Mục lục:
Bảng tuần hoàn hóa học chương trình mới
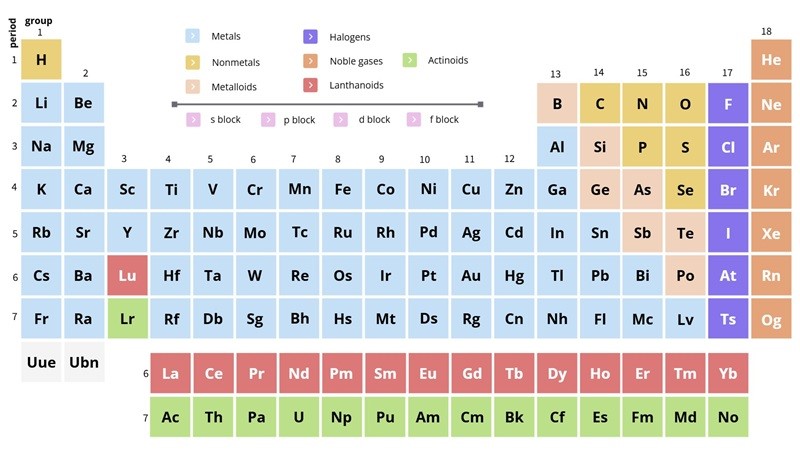
Bảng tuần hoàn hóa học chương trình mới được sắp xếp theo số hiệu nguyên tử tăng dần (tức số proton). Các hàng ngang (chu kỳ) thể hiện sự lấp đầy lớp electron, còn các cột dọc (nhóm) tập hợp các nguyên tố có tính chất hóa học tương tự.
Theo cơ học lượng tử, cấu hình electron chia bảng thành các khối s, p, d và f. Các bảng in thường hiển thị ký hiệu nguyên tố, số hiệu nguyên tử, và đôi khi có thêm khối lượng nguyên tử, cấu hình electron, độ âm điện, và số hóa trị phổ biến.
Trong 117 nguyên tố đã xác nhận, một số nguyên tố như techneti (43) và prometi (61) là nhân tạo dù có số hiệu nhỏ hơn urani (92). Nguyên tố neptuni (93) và plutoni (94) được xếp vào nhóm nhân tạo, nhưng vẫn tìm thấy với lượng rất nhỏ trong tự nhiên.
Tính tuần hoàn trong tính chất hóa học
Giá trị cốt lõi của bảng tuần hoàn là khả năng dự đoán tính chất hóa học của nguyên tố dựa trên vị trí của nó. Tuy nhiên, các tính chất này thay đổi khác nhau theo chiều ngang và chiều dọc – tức là dọc theo nhóm và ngang theo chu kỳ.
Nhóm và chu kỳ
Nhóm là cột dọc trong bảng tuần hoàn các nguyên tố.
Nhóm được xem là cách phân loại nguyên tố quan trọng nhất. Trong một số nhóm, các nguyên tố có tính chất rất giống nhau và biểu hiện xu hướng rõ rệt theo chiều dọc, vì vậy chúng thường được đặt tên thông dụng (không theo hệ thống), ví dụ: kim loại kiềm, kim loại kiềm thổ, halogen, và khí hiếm. Một số nhóm khác như nhóm 14 và 15 ít có điểm chung hoặc xu hướng rõ rệt, nên chỉ được gọi theo số nhóm.
Chu kỳ là hàng ngang trong bảng tuần hoàn.
Dù phân loại theo nhóm là phổ biến hơn, nhưng ở một số khu vực như khối d (kim loại chuyển tiếp) và đặc biệt là khối f (gồm họ lanthan và actin), các xu hướng và tính chất theo chiều ngang (chu kỳ) lại rõ ràng và quan trọng hơn so với theo nhóm.
Xu hướng tuần hoàn theo nhóm
Theo lý thuyết cơ học lượng tử hiện đại, các nguyên tố cùng nhóm có cấu hình electron lớp ngoài cùng (valence shell) giống nhau, điều này giải thích tại sao chúng có tính chất tương tự.
Các nguyên tố trong cùng nhóm cũng có xu hướng giống nhau về:
- Bán kính nguyên tử: tăng dần từ trên xuống do số lớp electron tăng → electron nằm xa hạt nhân hơn.
- Năng lượng ion hóa: giảm dần từ trên xuống vì electron dễ bị tách ra hơn do lực hút yếu hơn từ hạt nhân.
- Độ âm điện: cũng giảm từ trên xuống, do khoảng cách giữa electron hóa trị và hạt nhân tăng lên, khiến lực hút yếu hơn.
Xu hướng tuần hoàn theo chu kỳ
Các nguyên tố trong cùng chu kỳ thể hiện xu hướng biến đổi về:
- Bán kính nguyên tử: giảm dần từ trái sang phải. Lý do là mỗi nguyên tố thêm 1 proton và 1 electron → electron bị hút gần hơn về phía hạt nhân.
- Năng lượng ion hóa: tăng dần từ trái sang phải. Do nguyên tử càng nhỏ, electron càng bị hút chặt → cần nhiều năng lượng hơn để tách electron.
- Độ âm điện: cũng tăng theo chiều trái sang phải, vì lực hút của hạt nhân với electron mạnh hơn.
- Ái lực electron: cũng có xu hướng tăng nhẹ trong chu kỳ. Các kim loại (bên trái) thường có ái lực electron thấp, trong khi phi kim (bên phải) có ái lực cao hơn, trừ khí hiếm (vốn đã ổn định).
Các nhóm nổi bật trong bảng tuần hoàn chương trình mới
Khí hiếm (Noble gases)
Tất cả các nguyên tố thuộc nhóm 18 – còn gọi là khí hiếm – đều có lớp electron ngoài cùng bão hòa. Vì đã ổn định, chúng hầu như không cần phản ứng với các nguyên tố khác để đạt cấu hình bền, nên tính phản ứng rất thấp so với các nhóm khác.
Heli là nguyên tố trơ nhất, vì trong nhóm khí hiếm, tính phản ứng tăng dần theo chu kỳ (tức là các khí hiếm nặng hơn có thể phản ứng trong một số điều kiện, do có lớp vỏ electron lớn hơn). Tuy vậy, mức độ phản ứng của chúng vẫn rất thấp nói chung.
Halogen
Nhóm 17, hay halogen, gồm các nguyên tố thiếu 1 electron để đạt lớp vỏ ngoài cùng bão hòa. Do đó, chúng có xu hướng thu nhận electron trong phản ứng hóa học – đặc tính này gọi là độ âm điện.
Halogen có độ âm điện cao, đặc biệt là fluor – nguyên tố có độ âm điện cao nhất bảng tuần hoàn. Độ âm điện giảm dần theo chu kỳ từ trên xuống.
Tất cả halogen đều tạo thành axit với hydro, như:
- HF (axit flohydric)
- HCl (axit clohydric)
- HBr (axit bromhydric)
- HI (axit iodhydric)
→ Công thức chung: HX
Tính axit tăng theo chu kỳ, vì ion halogen nặng hơn (như I⁻) ổn định hơn trong dung dịch so với ion nhẹ (F⁻), do khối tích lớn hơn giúp phân tán điện tích tốt hơn.
Kim loại chuyển tiếp (Transition metals)
Thuộc nhóm 3 đến 12, kim loại chuyển tiếp thể hiện xu hướng cả theo chiều ngang lẫn chiều dọc trong bảng tuần hoàn. Tuy nhiên, sự khác biệt giữa các nhóm liền kề không quá lớn.
Phản ứng của kim loại chuyển tiếp thường liên quan đến các phức chất (coordinated species) – dạng mà nguyên tử kim loại liên kết với nhiều phân tử hoặc ion xung quanh.
Họ lanthan và actini (Lanthanides & Actinides)
Các nguyên tố thuộc họ lanthan (57–71) và họ actini (89–103) có tính chất hóa học rất giống nhau, thậm chí còn giống nhau hơn cả các kim loại chuyển tiếp.
Điều này khiến việc tách riêng chúng trong hỗn hợp rất khó khăn – điều đặc biệt quan trọng trong quá trình tinh chế urani phục vụ năng lượng hạt nhân.
Cấu trúc của bảng tuần hoàn hóa học
Yếu tố chính quyết định tính chất hóa học của một nguyên tố là cấu hình electron, đặc biệt là các electron ở lớp ngoài cùng (electron hóa trị).
Ví dụ, các nguyên tử có 4 electron hóa trị nằm ở orbital p sẽ thể hiện những đặc điểm tương tự nhau.
Loại orbital chứa các electron ngoài cùng xác định khối (block) mà nguyên tố thuộc về, còn số electron hóa trị quyết định nhóm (group) của nguyên tố.
Tổng số lớp electron trong nguyên tử sẽ xác định chu kỳ (period) mà nguyên tố đó nằm trong. Mỗi lớp electron gồm nhiều phân lớp (subshell), được lấp đầy theo nguyên tắc Aufbau – theo thứ tự năng lượng tăng dần như sau:
| Phân lớp | S | G | F | D | P |
| Chu kỳ 1 | 1s | ||||
| Chu kỳ 2 | 2s | 2p | |||
| Chu kỳ 3 | 3s | 3p | |||
| Chu kỳ 4 | 4s | 3d | 4p | ||
| Chu kỳ 5 | 5s | 4d | 5p | ||
| Chu kỳ 6 | 6s | 4f | 5d | 6p | |
| Chu kỳ 7 | 7s | 5f | 6d | 7p | |
| Chu kỳ 8 | 8s | 5g | 6f | 7d | 8p |
Chính cấu trúc này tạo nên hình dạng bảng tuần hoàn hiện nay. Vì các electron lớp ngoài cùng quyết định tính chất hóa học, nên các nguyên tố có cùng số electron hóa trị được xếp cùng một nhóm.
Do tầm quan trọng của lớp electron ngoài cùng, người ta chia bảng tuần hoàn thành các khối (blocks), đặt tên theo phân lớp chứa electron cuối cùng:
Ví dụ: khối s, khối p, khối d, khối f,…
Thông tin liên hệ:
- Trang web: https://bangtuanhoan.com/
- Địa chỉ: 618 Lê Trọng Tấn, P. Bình Hưng Hòa, Q. Bình Tân, TP HCM
- Hotline: 0936 292 319
- Email: lienhe@bangtuanhoan.com
Xem thêm:
